Contoh Soal Reaksi Pembatas. Ternyata, s lebih kecil daripada f2, sehingga dapat dipastikan bahwa reaktan yang habis adalah s dan s bertindak sebagai reaksi pembatas. Penentuan jumlah mol zat hasil reaksi berdasarkan pada jumlah mol zat pereaksi yang habis bereaksi. Tentukan massa gas amonia ($\mbox{nh}_{3}$) yang terbentuk jika dari percampuran gas tersebut terjadi reaksi! Rangkuman materi disertai 40 contoh soal laju reaksi kelas 11 dan jawaban berikut video pembelajaran dan latihan soal.

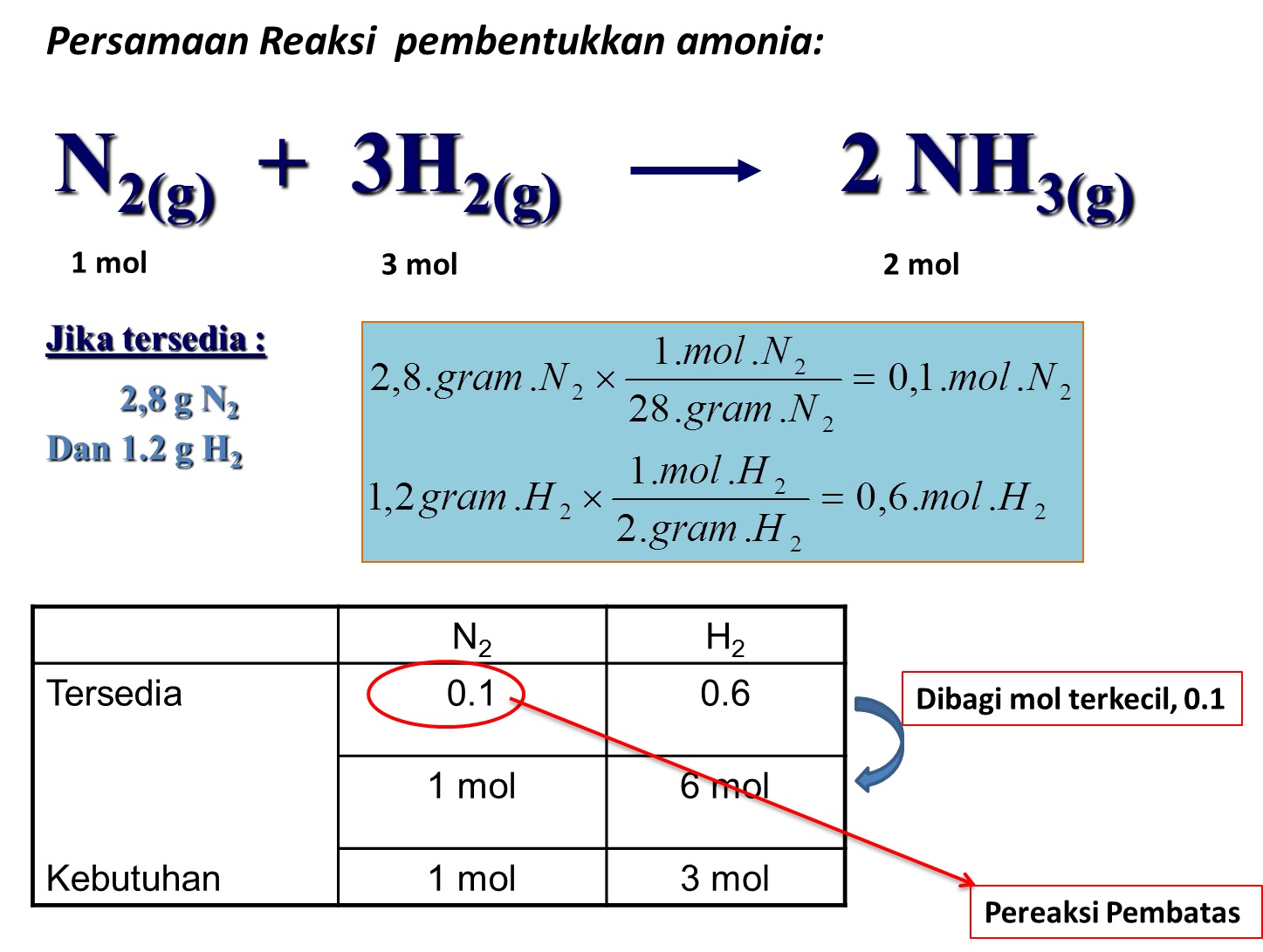
Tentukan massa gas amonia ($\mbox{nh}_{3}$) yang terbentuk jika dari percampuran gas tersebut terjadi reaksi! Contoh soal penentuan pereaksi pembatas dan pemkoreksiannya. Contoh persamaan reaksi pada contoh soal 1. Soal stoikiometri kelas x sma rangkuman materi, contoh soal konsep mol. Agar kalian semakin memahami pernyataan tersebut, perhatikan contoh soal perhitungan kimia dan jawaban berikut ini. A, b, dan c adalah koefisien reaksi, sedangkan a dan b adalah pereaksi (reaktan) dan c adalah hasil reaksi (produk).
Mol f2/koefisien = 2/1 :
Contoh soal 4 sebanyak 22 gram c 3 h 8 direaksikan dengan 48 gram o 2 berdasarkan persamaan reaksi berikut. Berdasarkan reaksi yang terjadi, maka dapat ditentukan reaktan yang habis adalah sebagai berikut. Contoh persamaan reaksi pada contoh soal 1. Oleh karena itu, jumlah mol nh 3 dihitung berdasarkan jumlah mol h 2. Inilah pembahasan lengkap terkait contoh. Mol f2/koefisien = 2/1 :

0,5 mol mg(oh) 2 bereaksi dengan 0,5 mol hcl sesuai persamaan reaksi: Untuk mengetahui dan menghitung hubungan kuantitatif suatu reaksi kita perlu memahami tentang konsep mol. Pereaksi yang habis bereaksi (pereaksi pembatas) adalah pereaksi yang jumlah molnya terkecil, yaitu h 2. Penentuan jumlah mol zat hasil reaksi berdasarkan pada jumlah mol zat pereaksi yang habis bereaksi. Contoh persamaan reaksi pada contoh soal 1.
 Source: theadorableabdul.blogspot.com
Source: theadorableabdul.blogspot.com
Pereaksi pembatas sanggup ditentukan dengan membagi jumlah mol dengan koefisien pereaksinya kemudian memilih nilai yang paling kecil. Contoh soal 4 sebanyak 22 gram c 3 h 8 direaksikan dengan 48 gram o 2 berdasarkan persamaan reaksi berikut. Berikut ini adalah beberapa contoh soal untuk menghitung pereaksi pembatas: Video pembelajaran diberikan dengan gaya yang enak dan mudah dipahami. Aa + bb → cc.
 Source: youtube.com
Source: youtube.com
Ch 4 (g) + 2o 2 (g) → co 2 (g) + h 2 o (g) tentukan senyawa yang menjadi pereaksi pembatas! Logam alkali (golongan 1) bereaksi dengan halogen (golongan 17. A, b, dan c adalah koefisien reaksi, sedangkan a dan b adalah pereaksi (reaktan) dan c adalah hasil reaksi (produk). Setelah pereaksi pembatas habis, tidak ada lagi produk reaksi yang terbentuk. 45+ soal penyetaraan reaksi redoks pilihan ganda [+pembahasan] oleh anas ilham diposting pada mei 9, 2021.

Pereaksi pembatas sanggup ditentukan dengan membagi jumlah mol dengan koefisien pereaksinya kemudian memilih nilai yang paling kecil. Tuliskan persamaan reaksi setara untuk reaksi kimia zn +. Rangkuman materi disertai 40 contoh soal laju reaksi kelas 11 dan jawaban berikut video pembelajaran dan latihan soal. 1 amonia dapat dibuat melalui reaksi: Pembahasan soal kimia nomor 34 sbmptn 2018 semua kode soal.
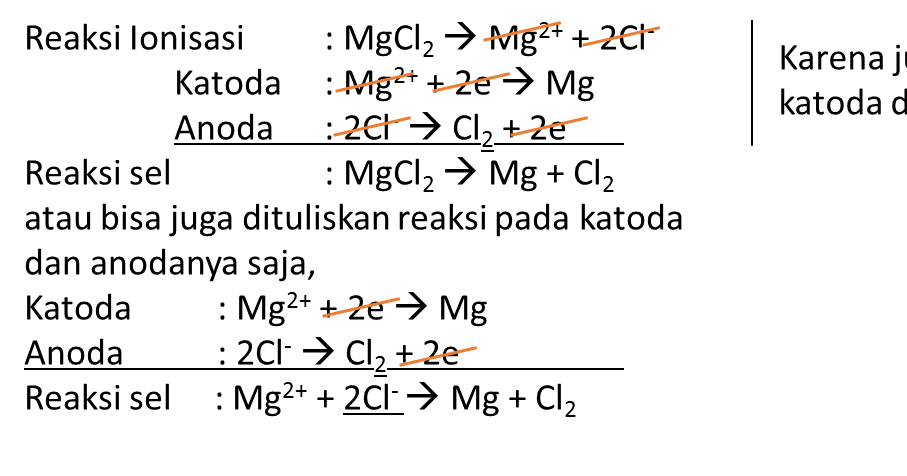 Source: nixonselly.blogspot.com
Source: nixonselly.blogspot.com
Ch 4 (g) + 2o 2 (g) → co 2 (g) + h 2 o (g) tentukan senyawa yang menjadi pereaksi pembatas! Contoh persamaan reaksi pada contoh soal 1. Untuk lebih jelasnya, pelajari pemkoreksian tumpuan soal pereaksi pembatas dibawah ini. Pereaksi pembatas sanggup ditentukan dengan membagi jumlah mol dengan koefisien pereaksinya kemudian memilih nilai yang paling kecil. Jadi, jumlah pereaksi pembatas menentukan jumlah produk yang dihasilkan.
 Source: contoh-contoh-soal.blogspot.com
Source: contoh-contoh-soal.blogspot.com
Jumlah mol o 2 /koefisien reaksi o 2 = 4/3 = 1,33 mol. Jadi, jumlah pereaksi pembatas menentukan jumlah produk yang dihasilkan. Ch 4 (g) + 2o 2 (g) → co 2 (g) + h 2 o (g) tentukan senyawa yang menjadi pereaksi pembatas! Cari pereaksi pembatas dan pereaksi berlebih ketika 0,5 mol zn bereaksi dengan 0,4 mol hcl. Jumlah mol o 2 /koefisien reaksi o 2 = 4/3 = 1,33 mol.
 Source: latihansoalyuk.blogspot.com
Source: latihansoalyuk.blogspot.com
Oleh karena itu, jumlah mol nh 3 dihitung berdasarkan jumlah mol h 2. Untuk soal yang berkaitan dengan pereaksi pembatas, menentukan terlebih dahulu zat yang bertindak sebagai pereaksi pembatas, yaitu jika jumlah mol pereaksi yang diketahui dibagi koefisien pada persamaan reaksi memberikan nilai lebih kecil dibanding pereaksi lainnya, maka pereaksi tersebut merupakan pereaksi pembatas. Diketahui mr metana = 16, ar oksigen = 16, dan mr h 2 o = 18. Pereaksi yang habis bereaksi (pereaksi pembatas) adalah pereaksi yang jumlah molnya terkecil, yaitu h 2. Mol mgcl 2 dan mol h 2 o.
 Source: materikimia.com
Source: materikimia.com
A direaksikan dengan b membentuk c menurut persamaan reaksi: 45+ soal penyetaraan reaksi redoks pilihan ganda [+pembahasan] oleh anas ilham diposting pada mei 9, 2021. Suatu reaksi berlangsung sesuai persamaan reaksi berikut: Logam alkali (golongan 1) bereaksi dengan halogen (golongan 17. Tentukan massa gas amonia ($\mbox{nh}_{3}$) yang terbentuk jika dari percampuran gas tersebut terjadi reaksi!
This site is an open community for users to do submittion their favorite wallpapers on the internet, all images or pictures in this website are for personal wallpaper use only, it is stricly prohibited to use this wallpaper for commercial purposes, if you are the author and find this image is shared without your permission, please kindly raise a DMCA report to Us.
If you find this site adventageous, please support us by sharing this posts to your own social media accounts like Facebook, Instagram and so on or you can also save this blog page with the title contoh soal reaksi pembatas by using Ctrl + D for devices a laptop with a Windows operating system or Command + D for laptops with an Apple operating system. If you use a smartphone, you can also use the drawer menu of the browser you are using. Whether it’s a Windows, Mac, iOS or Android operating system, you will still be able to bookmark this website.





